病理検体の目的外使用に関する提言
平成14年3月
社団法人日本病理学会
倫 理 委 員 会
理 事 会
1. 病理検体を用いた学術研究・医学教育を行うにあたっては、患者や家族の
自己決定権の担保、個人情報やプライバシーの保護・管理、人権や利益の専
童がなされなければならない。これらの倫理的要件を保証する上で、病理検
体の管理者である病理医は重要な役割を担っている。従って、所属する施設
でそれを具現するべく積極的に発言し、努力する責務がある。
2. 病理検体を学術研究や医学教育に使用する際には、原則として事前に患者
本人や代諾者(親権者や親族等)から文書による同意を得る必要がある。
さかのぼって同意の得られない病理検体では倫理委員会など、第三者により
研 究計画が検証・評価されなくてはならない。
3. 病理検体の目的外使用に関する承諾手続きは、各医療施設の実状に沿った
方法で運用されるべき、と思料される。病理検体以外の残余検体(血液・尿
など)やレントゲンフィルム、肉眼写真などと同時に、包括的同意を得るこ
とも有効である。
この際、個人情報の保護、臓器・検体の取り扱いと保管、学術研究や医学
教育への使用、倫理的配慮等について記載し、同意を求める。
4. 病理解剖標本を除く病理検体に開する法的規制やガイドラインは示されて
いないが、診断書、顕微鏡標本、パラフィン・ブロックあるいは肉眼写真の
保管等は病理解剖標本と同等に扱われるべきである。
なお、病理組織診断終了後の臓器・組織あるいは顕微鏡標本は患者本人に
帰属する。従って、返却を求められた場合は、それに応じる必要がある。
5. 最も重要なことは、病理診断業務の意義と内容について不断の啓蒙活動を
行うことである。社会の理解が進めば、病理業務の円滑な運営と学術研究・
医学教育への貢献が担保される。
【背景】
医学研究や医療の新たな展開に伴って、倫理的観点に関する配慮が求められている。具体的には1)インフォームド・コンセントの徹底、2)自己決定権の担保、3)個人情報やプライバシーの保護・管理、4)患者の人権や利益の尊重等に集約される。他方、個人情報に基づく疫学研究や情報公開の重要性が強調されており、医療現場に多少の戸惑いや混乱が生じている現状は見逃せない。病理診断業務の現場においては病理検体の目的外使用に関する多少の混乱と誤解が生じている。具体的には、切除標本の残余組織、パラフィン・ブロックや凍結組織、顕微鏡標本(組織標本、細胞診標本)、肉眼・顕微鏡写真等を学術研究・医学教育へ利用可能とする範囲と手続きが問題視されている。
そこで、社団法人日本病理学会理事会は平成12年11月に「病理検体を学術研究、医学教育に使用することについての見解」1)を提示した。本見解は日本病理学会会員に広く受け入れられている、と忖度される。さらに、平成13年6月には本学会に倫理委員会が設置され、平成13年11月27日には秋期総会において、「病理解剖の倫理的課題に関する提言」を示した2)。今回、病理解剖を除く病理検体の目的外使用に関する現状を把握し、現時点における提言を倫理委員会の立場から取りまとめた。
【現状把握】
日本病理学会が2001年8月に実施したアンケート調査では、病理検体の目的外使用のために文書で承諾を得ているのは51施設中14施設(27.5%)に留まっている(資料1-[1])。検討中の21施設(31.2%)では目的外使用に関して、「ヒトゲノム・遺伝子解析研究に関する倫理指針」3)における試料等の分類のB群試料に相当する承諾を想定している(表)。手術や剖検時点において、病理検体がいかなる研究に用いられるかは推定出来ないからである。
承諾のない検体はC群試料に含まれる。C群試料であっても、倫理委員会の承認を得れば、研究・教育への使用は可能である。この点に関するアンケート調査では、倫理委員会に承認を得る予定がないとしたのは8施設(15.7%)のみであり、今後は申請あるいは研究内容により申請すると返答した施設は39施設(74.5%)であった。大半の施設が倫理委員会の重要性を認識しているが、見解が統一されているとは言い難い(資料1-[2])。なお、今回のアンケートでは調査されていないが、大学医学部を除けば、倫理委員会の設置されていない病院に勤務する病理医は少なくないことが予測される。
【指針やガイドライン】
病理検体の取り扱いや目的外使用の承諾は病理解剖と手術ないし生検標本では明らかに異なる。前者は遺族の同意となるが、後者では本人からの同意が可能である。しかしながら、「死体解剖保存法」や「病理解剖指針について(通知)」等により規定されている病理解剖とは異なり、手術・生検標本については保存等の取り扱いや目的外使用に関する法的根拠は暖味である。
平成9年12月に厚生大臣から、厚生科学審議会に「手術等で摘出されたヒト組織を用いた研究開発の在り方について」が諮問され、平成10年12月に答申されている4)。本答申は手術から得られた組織を用いた医薬品の研究開発を念頭に置いたものであり、病理検体やパラフィン・ブロック、組織・細胞標本は直接的な対象とはなっていない。ただし、提供者への十分な情報開示と同意、個人情報の保護は謳われており、社会的常識、倫理的観点からも手術標本やパラフィン・ブロック、組織標本等を学術研究や医学教育に使用する際には、十分な配慮が必要である。
個人情報保護法(案)は生存している個人の情報が対象となる。学術研究は除外されているが、適正な取り扱いが求められている。なお、本法案は国会で継続審議となっているが、ジャーナリズムの立場からは反対意見が多く、成立の見通しはたっていない。
【病理検体の取り扱いにおける倫理的配慮】
病理医は病理診断により疾病に関する重要な情報を提供し、医療の質を検証する立場にある。剖検で得られる標本を除けば、病理検体は大きく2つのカテゴリーに分類される;(1)病変の診断を目的とした生検標本および細胞検体、(2)治療目的で切除された手術標本(肉眼写真を含む)。こうした検体を用いて多種多様な医学研究が展開され、その成果は臨床の場に活かされ、医学・医療の発展に貢献してきた。医学教育への寄与も大きい。こうした潮流が阻害されるべきではない。しかし、一義的な病理・細胞診断を除けば、学術研究や医学教育への利用は検体の目的外使用となる。
本倫理委員会で検討された項目は、以下の如く要約される。
(1)病理組織診断終了後の臓器・組織あるいは顕微鏡標本の所有権は患者本人や家族に帰属する。この点に関しては法的根拠が希薄であるが、病理解剖標本と同様に扱われべきである。従って、返却を求められた場合は、それに応じる必要があるが、大切なことは病理業務の重要性を社会に訴え、不断の啓蒙活動を実施することであろう。
(2)症例報告を含む学術研究や医学教育への活用は推進されるべきである。成果発表に際しては、個人の同定が可能な情報を提示してはならない(連結不可能匿名化)。この点に関しては、平成13年11月27日に日本病理学会が提示した「症例報告における患者情報保護に関する指針」2)を本委員会は全面的に支持する。
(3)病理検体を学術研究や教育目的で使用するには、原則として事前に患者本人や代諾者(親権者や親族等)から文書による同意を得る必要がある。ただし、同意を得るのは臨床医ないし主治医であって、病理医ではない。この点に関しては、幾つかの問題を含んでおり、次の【現状と対策】で別個に触れる。
(4)さかのぼって同意の得られない検体では倫理委員会など、第三者による研究計画の検証が必要である。倫理委員会が設置されていない施設では、施設長や病院長により検証されるべきである。
(5)大切なことは倫理審査の結果ではなく、第三者による検証を求める姿勢である。
(6)ゲノム・遺伝子解析研究は三省合同の指針3)に従って計画・実施される。
【現状と対策】
前述の如く、残余組織や顕微鏡標本などの病理検体を学術研究や医学教育へ利用する際には、本人もしくは代諾者の同意が必要となるが、それを得るのは臨床医ないし主治医である。この点に関しては、以下の問題点が指摘され、議論された。
(1)同意もしくは承諾を得ることは必要であるが、手続きや書式をいたずらに煩雑にすると、医療現場から受け入れられない。患者にとっても負担が少なくない。
(2)生検標本と手術標本を同一に扱うことが出来るか。生検検査は1度とは限らず、毎回必要であろうか。手術標本では少なくとも病理検体を学術研究や医学教育へ利用することを「手術承諾書」に盛り込むことが可能である。
(3)患者のサイドに立てば、病理検体に限らず、残余血液、尿、レントゲン・フィルム等も目的外使用における同意・承諾が必要なものである。従って、病理検体のみを別個に扱うことには慎重であるべき、と思慮される。
(4)顕微鏡標本やパラフィンブロック等の病理検体の所有権を受診施設へ委譲すること、廃棄や火葬に関する承諾も得る必要がある。
(5)以上の観点から、病理検体を学術研究や医学研究に使用する際には、患者や代諾」者の同意・承諾が必要であるが、その運用は各施設の実状に沿った、実効あるものとするべきである。
本倫理委員会は平成13年11月27日に「病理解剖の倫理的課題に関する提言」を提示した。その際、「病理解剖に関する遺族の承諾書」をモデルとして付記した。今回、承諾書のモデルは敢えて提示しない。既に平成12年11月29日に日本病理学会理事会は「病理検体を学術研究、医学教育に使用することについての見解」1)を提示し、同意書のモデルを示しているからである。加えて、各施設の実状に沿った同意書・承諾書を臨床サイドとの共同作業により作成すべき、と思料された。
なお、全国アンケートからは切除標本、生検標本あるいは細胞検体などの病理検体の説明を同意書に組み入れたものと、別個にしたものがあった。同意書の作製にあたって参考となると考えられるので、幾つかの施設におけるものを資料として添付する。
【まとめ】
医学研究や教育のためとはいえ、これまで病理検体の目的外使用や検体の管理に関しては、やや杜撰な面があったことは否めない。今後は人権の尊重やプライバシー保護面から、病理検体を研究や教育に使用することを事前に書面で承諾を得る必要がある。昨今、提示されている各種の指針は研究や教育の展開を阻害するものではない。定められた手続きを踏めば、言われなき中傷・誹誇から病理医を含む医療従事者や研究者を保護する役割も担っているのである。
倫理的問題が生じた場合の基本的原則:「一人で決めない、一度に決めない」
1) 社団法人日本病理学会理事会:病理検体を学術研究、医学教育に使用することについての
見解:日本病理学会会報158号、1〜2、2000年12月
2) 社団法人日本病理学会平成13年度秋期総会資料、pp9〜14
3) 文部科学省ホームページ:「ヒトゲノム・遺伝子研究に関する倫理指針」
http://www.mext.go.jp/a_menu/shinkou/seimei/index.htm
4) 厚生省:手術等で摘出されたヒト組織を用いた研究開発の在り方について(答申)1998年12月
表1:「ヒトゲノム・遺伝子解析研究における倫理指針」で示された試料等の分類
A群試料等 試料等の提供時に、ヒトゲノム・遺伝子解析研究における利用を含む同意
が与えられている。
B群試料等 試料等の提供時に、ヒトゲノム・遺伝子解析研究における利用が明示され
ていない研究についての同意のみが与えられている
C群試料等 試料等の提供時に、研究に利用することの同意が与えられていない
日本病理学会が2001年8月に実施したアンケート調査
資料1一[1]:生検や手術材料を教育・研究に使用することに関する承諾について
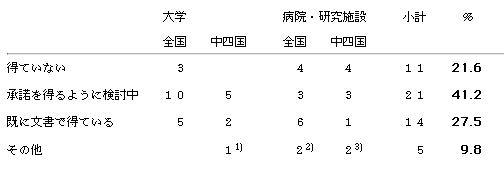
1) 承諾を得ている科と得ていない科があり、対応が統一していない
2) 承諾書の修正案を病院長に提示しているが、保留となっている
遺伝子検索に限って承諾を得ている
3) 臓器や症例によっては承諾を得ている
気管支鏡検査の承諾書に含まれている。その他の臓器に関しては倫理委員会に申請す
ることで対応
主な意見:
-
ゲノム解析研究に限らず、承諾を得るのは病理医の責務
-
臨床の意識が希薄
-
ゲノム解析関連は統一されたものが作製された
-
個々の科で対応している。病理関係も臨床科にお願いしている
-
関連大学からの依頼が主で、臨床医が対応している
-
計画された特定の研究に関しては承諾を得ている。臓器写真を教育や講演で使用する場合、匿名化しているが承諾は得ていない
-
診療と教育・研究の領域に重複があり、境界が不明瞭であるため承諾なしで利用されているのが現状。臨床医の意識は低い
資料1一[2]:凍結材料あるいはパラフィンブロック等を用いた研究を実施する際の
倫理委員会における審査(目的外使用)

1) 目的外使用であり、原則として全ての研究で審査が必要。簡便な審査を実施
2) 対応を検討中
3) 全ての研究を申請
4) 臨床科が申請し、病理の意見聴取なしにパラフィン切片を提供した。一般病院
では倫理委員会が機能しているとは限らない
主な意見
-
遺伝子関連は必ず申請
-
目的外使用であり、原則として全ての研究で審査が必要。簡便な審査を実施
-
現在は遺伝子関連のみ、将来的にはすべての研究を申請するよう指導中
-
他施設へ資料を貸し出すことは厳しい時代
-
新潟市では病理標本は個人情報とされていない。目的外使用であり、倫理委員会に諮る
ホームへ戻る


